29 de dezembro de 2011
21 de dezembro de 2011
Novos aparelhos de controle de insulina e glicose vão revolucionar tratamento do diabetes
A agência americana para drogas e alimentos, Food and Drug Administration
(FDA), aprovou diretrizes para permitir a entrada no mercado de um dispositivo
potencialmente revolucionário no tratamento de diabetes tipo 1. A decisão veio
depois de meses de negociações com defensores dos pacientes, fabricantes de
dispositivos médicos e pesquisadores universitários, que trabalham para
desenvolver um pâncreas artificial _ um complexo sistema de bombas e sensores
que visa a automatizar o tratamento do diabetes tipo 1.
_ Esta orientação do FDA vai acelerar a chegada ao mercado do pâncreas
artificial. O importante é garantir que o produto que chega ao mercado será
seguro e eficaz _ avaliou Charles Zimliki, representante da agência.
A agência deu aos pesquisadores e fabricantes de aparelhos médicos
orientações claras para a aprovação de ensaios clínicos, a fim de assegurar a
prova que são seguros em ambientes do mundo real ambulatorial.
O médico Jeffrey Shuren, diretor do Centro do FDA para Dispositivos e Saúde
Radiológica, disse que o pâncreas artificial vai mudar a vida de milhões de
pessoas.
_ A chegada de um dispositivo como este ao mercado poderia mudar a vida de
milhões de pessoas com diabetes, e queremos que segurança e eficácia de revisão
possam dar aos pacientes a confiança de que o dispositivo funciona _ disse
Shuren.
Os dispositivos existentes hoje envolvem uma característica de segurança: são
construídos com uma bomba de insulina que desliga automaticamente quando o
açúcar do sangue de um diabético cai para níveis perigosamente baixos. Os novos
dispositivos são mais complexos, de modo a automatizar muitas das funções do
pâncreas, facilitando a tarefa de controlar a doença.
Estes novos sistemas são compostos de aparelhos médicos usados fora do
corpo para assumir o controle da insulina, já que células do pâncreas são
destruídas em pessoas com diabetes tipo 1. Os novos sistemas também combinam
dois dispositivos médicos, uma bomba de insulina e uma outra, contínua, para
monitorar o nível de glicose (ou CGM). Este monitor recebe informações sobre os
níveis de glicose no sangue a partir de um sensor colocado sob a pele do
paciente.
A bomba e CGM trabalham juntos, permitindo a monitorização dos níveis da
glicose do corpo e, automaticamente, o bombeamento de doses adequadas de
insulina, conforme determinado por um algoritmo de computador.
Estes sistemas são feitos para gerenciar picos e baixas perigosos do açúcar
no sangue, que ocorrem com diabéticos que tentam controlar a doença, verificando
a sua de açúcar no sangue e injetando-se com insulina.
O documento de orientação do FDA recomenda uma progressão de três fases de
ensaios clínicos, incluindo ensaios clínicos ambulatoriais, para aprovação dos
novos aparelhos. E sugere maneiras pesquisadores podem usar a segurança e os
dados de eficácia existentes para vários componentes que compõem o sistema,
incluindo os dados recolhidos a partir de estudos clínicos realizados fora de os
EUA. Ao final, a agência vai examinar os pedidos de aprovação de produtos.
Os novos dispositivos são destinados a tratar a 3 milhões de americanos com
diabetes tipo 1, doença auto-imune na qual o sistema imunológico destrói as
células no pâncreas que produzem insulina. O diabetes tipo 1 é menos comum do
que o diabetes tipo 2, forma da doença associada à obesidade e falta de
exercício, que afeta 26 milhões de pessoas nos Estados Unidos. Pessoas com
diabetes tipo 1 devem monitorar o açúcar no sangue e tomar insulina várias vezes
ao dia para regulá-los e prevenir complicações do diabetes, que incluem doenças
cardíacas e renais.
Diabetes: Investigadores da UC dão importante passo para a insulina oral
Uma tecnologia desenvolvida por
uma equipa internacional de investigadores, coordenada pelos portugueses António
Ribeiro e Francisco Veiga, da Faculdade de Farmácia da Universidade de Coimbra
(UC), já garantiu a protecção em ambiente gástrico e uma passagem de insulina
através do epitélio intestinal de ratos acima de 30 por cento, um nível de
biodisponibilidade sem precedentes, segundo foi hoje (dia 20) anunciado.
Para que a administração oral de insulina possa vir a ser uma realidade
terapêutica para a Diabetes, com melhorias significativas da qualidade de vida
dos doentes, a comunidade científica tem, num labirinto de interacções, dois
grandes desafios: garantir a protecção da insulina em ambiente gastrintestinal e
conseguir que atravesse o epitélio intestinal (barreira teoricamente impermeável
à passagem de moléculas como a insulina).
Fazendo uma analogia, “perante um
imponente muro, praticamente impossível de derrubar, a estratégia adoptada pela
nossa equipa, e que passa por um sistema de micro e nanopartículas já protegido
por duas patentes, conseguiu passar o muro”, explica António Ribeiro.
Apesar de ser considerado um
“passo de gigante” para o transporte de insulina, o investigador da UC adverte
que “não basta passar o muro. Temos de fazer novos estudos para mostrar como o
conseguimos, ou seja, quais foram os mecanismos que permitiram essa
passagem”.
Nesse sentido, os últimos estudos
desta tecnologia concebida pelos investigadores de Coimbra, composta por um
sistema de micro e nanopartículas, construídas à base de biopolímeros -
proteínas e polissacarídeos - para administração oral de insulina, revelaram, in
vitro, que a insulina encapsulada atravessa o epitélio intestinal por duas vias:
isolada e revestida.
Os resultados agora alcançados
foram obtidos por uma vasta equipa, que além dos coordenadores, António Ribeiro
e Francisco Veiga, envolveu os investigadores Isabel Vitória, Rui Carvalho,
Camille Woitiski e contou ainda com a colaboração de equipas do Centro de
Investigação de Ciências da Saúde (CICS) e da Universidade de Queens
(Canadá).
Artigo em: Campeão - Jornal Online
14 de dezembro de 2011
Regulação da Glicémia
Apesar dos longos intervalos entre refeições ou do consumo ocasional de
refeições com uma carga pesada de carboidratos (por exemplo, metade de um bolo
de aniversário ou um pacote inteiro de batatas fritas), o nível glicémico em
humanos normalmente fica dentro de uma faixa estreita de valores.
Na maioria das
pessoas, os valores variam de 70 mg/dL a talvez 110 mg/dL (3,9-6,1 mmol/L),
exceto bem logo após de se alimentar, quando ocorre um aumento temporário da
glicemia. Em homens adultos saudáveis de cerca de 75 kg e com um volume de
sangue de 5 L, um nível glicêmico de 100 mg/dL ou 5,5 mmol/L corresponde a
aproximadamente 5 g de glicose no sangue e aproximadamente 45 g na água total do
organismo (neste caso, a água representa muito mais do que apenas sangue, já que
o corpo humano é feito de 60% de água, em peso).
Este efeito homeostático é
resultado de vários factores, sendo o mais importante a regulagem hormonal.
Existem dois grupos de hormônios metabólicos de efeitos antagônicos que afetam o
nível de glicose sanguíneo:
- hormônios catabólicos, por exemplo o glucagon, o hormônio do crescimento e as catecolaminas, que aumentam a glicemia, e;
- hormônios anabólicos - insulina -, que reduzem a glicemia.

Mecanismo de libertação de insulina, dependente de glicose
As células beta
presentes nas ilhotas de Langerhans são sensíveis a variações na glicemia por
causa dos seguintes mecanismos (veja a figura):
A glicose entra nas células beta pelo transportador de glicose GLUT2.
A glicose passa por glicólise e pelo ciclo respiratório, onde são produzidas
moléculas de ATP de alta energia por reações bioquímicas de oxidação.
Por ser dependente de ATP, que por sua vez originou-se de glicose proveniente
do sangue, os canais de potássio controlados por ATP fecham-se e a membrana
celular despolariza-se.
Sob despolarização, os canais de cálcio (Ca2+) controlados por voltagem
elétrica abrem-se e os íons de cálcio fluem para dentro das células.
O aumento do nível de cálcio ocasiona a ativação da fosfolipase C, que corta
o fosfolipídeo da membrana fosfatidil inositol 4,5-bifosfato em 1,4,5-trifosfato
e diacilglicerol
O inositol 4,5-bifosfato liga-se às proteínas receptoras no retículo
endoplasmático. Isto aumenta ainda mais a concentração de cálcio no interior da
célula.
O aumento significativo de cálcio na célula produz a liberação de insulina
previamente sintetizada, que tinha sido armazenada em vesículas secretoras.
O nível de cálcio também controla a expressão do gene de insulina via
proteína Ligante de Elemento Responsivo a Cálcio (em inglês, CREB).
Este é o mecanismo principal de libertação de insulina e regulagem de síntese
de insulina. Adicionalmente, certa parte da síntese e libertação de insulina
ocorre geralmente durante o consumo de alimentos, não apenas sob a presença de
glicose ou carboidratos no sangue, e as células beta são ainda influenciadas de
alguma forma pelo sistema nervoso autônomo.
A acetilcolina, liberada de
terminações nervosas do nervo vago (sistema nervoso parassimpático), a
colecistocinina, liberada por células enteroendócrinas da mucosa intestinal, e o
peptídeo inibitório gastrointestinal são algumas substâncias que estimulam a libertação de insulina.
O sistema nervoso simpático (agonistas adrenérgicos
alfa-2) pode inibir a libertação de insulina.
Quando a glicémia estabelece-se
nos valores fisiológicos normais, cessa ou diminui a libertação de insulina a
partir das células-beta. Se a glicémia cai abaixo desses valores, especialmente
a valores perigosamente baixos, a libertação de hormônios hiperglicemiantes
(principalmente glucagon, de células alfa) induz à disponibilização de glicose
ao sangue. A libertação de insulina é fortemente inibida pelo hormônio do
estresse, a adrenalina (epinefrina).
Fonte: http://www.marguitos.kit.net/saude/diabetes.html#insulina
Insulina: O que é?
É o hormônio responsável pela redução da glicemia
(taxa de glicose no sangue), ao promover o ingresso de glicose nas células. Ela
também é essencial no consumo de carboidratos, na síntese de proteínas e no
armazenamento de lipídios (gorduras).
É produzida nas ilhotas de Langerhans, células do pâncreas endócrino. Ela age em uma grande parte das células do organismo, como as células presentes em músculos e no tecido adiposo, apesar de não agir em células particulares como as células nervosas.
Quando a produção de insulina é deficiente, a glicose se acumula no sangue e na urina, matando as células de fome: é a diabetes mellitus. Para pacientes nessa condição, a insulina é provida através de injeções, ou bombas de insulina. Recentemente foi aprovado o uso de insulina inalada. Porém, ainda há controvérsias acerca do uso do produto comercializado pela Pfizer. A agencia de saude britanica nao recomenda seu uso.
A insulina é um polipeptídeo de estrutura química plenamente conhecida, e pode ser sintetizada a partir de diversos animais. Mais recentemente, surgiram os medicamentos análogos de insulina, que não são propriamente a insulina em si, mas moléculas de insulina modificadas em laboratório.
Insulina - Descoberta
Em 1905, Paul
Langerhans, um estudante de medicina em Berlin, estava estudando a
estrutura do pâncreas através de um microscópio quando percebeu células antes
desconhecidas espalhadas pelo tecido exócrino. A função da "pequena porção de
células", mais tarde denominada como ilhotas de Langerhans, era desconhecida,
mas Edouard Laguesse posteriormente sugeriu que tais
células poderiam produzir algum tipo de secreção que participasse no processo de
digestão.
Em 1889, o médico teuto-polonês Oscar Minkowski em colaboração com Joseph von Mehring removeu o pâncreas de um cão saudável para demonstrar o papel do órgão na digestão de alimentos. Vários dias após a remoção do pâncreas, o guarda do cão percebeu muitas moscas alimentando-se da urina do animal. Verificou-se com o teste da urina do cão que havia açúcar nela, o que demonstrou pela primeira vez a relação entre o pâncreas e a diabetes. Em 1901, outro passo importante foi alcançado por Eugene Opie, quando ele estebeleceu claramente a ligação entre as ilhotas de Langerhans e a diabetes: "Diabetes mellitus... é causada pela destruição das ilhotas de Langerhans e ocorre apenas quando tais células são em parte ou totalmente destruídas".
Durante as duas décadas seguintes foram feitas várias tentativas de isolamento da secreção das ilhotas como um tratamento potencial de diabetes. Em 1906, Georg Ludwig Zuelzer foi parciamente feliz no tratamento de cães com extrato pancreático, mas teve que interromper seus trabalhos. Entre 1911 e 1912, E. L. Scott da Universidade de Chicago usou extratos pancreáticos aquosos e notou uma leve diminuição da glicosúria, mas não conseguiu convencer o diretor da instituição dos resultados, e a pesquisa teve de ser encerrada. Israel Kleiner demonstrou efeitos similares na Rockfeller University em 1919, mas seu trabalho foi interrompido pela Primeira Guerra Mundial. Nicolae Paulescu, um professor de fisiologia da Escola Romena de Medicina, publicou um trabalho parecido em 1921 realizado na França e patenteado na Romênia, e discute-se desde então se Paulescu não tenha sido o verdadeiro descobridor da insulina.
Entretanto, o comitê do Prêmio Nobel em 1923 creditou a extração prática da insulina a uma equipe da Universidade de Toronto. Em outubro de 1920, Frederick Banting lia um dos artigos de Minkowski e concluiu que Minkowski estava mesmo é estudando secreções digestivas originalmente, e por isso não se conseguia extrair a insulina com sucesso. Ele redigiu uma nota para si mesmo: "Ligar duto pancreático do cão. Manter cães vivos até que acinos se degenerem, sobrando ilhotas. Tentar isolar secreção interna delas e aliviar glicosúria".
Ele viajou a Toronto para encontrar-se com J. J. R. Macleod, que não se impressionou plenamente com a idéia. De qualquer forma, Macleod deixou à disposição de Banting um laboratório da universidade, e um assistente, Charles Best, e dez cães enquanto saía de férias no verão de 1921. O método de Banting e Best era amarrar uma ligadura ao redor do duto pancreático dos cães e, várias semanas depois, examinar que as células digestivas pancreáticas tinham morrido e sido absorvidas pelo sistema imunológico, deixando milhares de ilhotas. Isolava-se a proteína dessas ilhotas para produzir o que vinham chamando de isletina. Banting e Best mantiveram um cão pancreatectomizado vivo durante todo o verão.
Macleod viu o valor da pesquisa na sua volta da Europa, mas pediu uma contraprova para saber se o método realmente funcionava. Várias semanas depois ficou claro que o segundo ensaio tinha sido um sucesso, e assim Macleod ajudou na publicação dos resultados em novembro daquele ano. Porém, precisavam de seis semanas para extrair a isletina, o que tornava o ensaio dramaticamente moroso. Banting sugeriu que tentassem usar pâncreas de feto de bezerro, que ainda não teria desenvolvido glândulas digestivas, e ficou alivado pelo sucesso da empreitada.
Com a solução para a fonte de isletina, faltava agora purificar a proteína. Em dezembro de 1921, Macleod convidou o brilhante bioquímico James Collip para ajudar na tarefa, e em um mês aprontaram-se para um teste.
| Foto: Informativo do Centro DB de educação em diabetes - Ano XXI - 76 - 2006 | ||
 Leonard com sua mãe em janeiro de 1922 |
 Meses após receber as aplicações de insulina |
 Leonard anos depois |
Em 11 de janeiro de 1922, Leonard Thompson, um
diabético de quatorze anos, recebeu a primeira injeção de insulina.
Infelizmente, o extrato estava tão impuro que ele acabou sofrendo uma reação
alérgica severa, e injeções adicionais foram canceladas. Durante os doze dias
seguintes, Collip trabalhou dia e noite para melhorar o extrato, e uma segunda
dose foi injetada no dia 23. Desta vez foi um sucesso, não apenas em não
apresentar efeitos colaterais, mas também por eliminar completamente os sintomas
de diabetes. Entretanto, Banting e Best não se davam bem com Collip, porque
aparentemente viam nele um intruso, e então Collip logo os deixou.
Durante a primavera de 1922, Best conseguiu melhorar as técnicas de preparo a ponto de poder extrair grandes quantidades de insulina, embora o extrato ainda permanecesse impuro. Contudo, eles receberam uma oferta de ajuda da Eli Lilly logo depois de suas publicações em 1921, e aceitaram-na em abril. Em novembro, a Lilly conseguiu a façanha de produzir grandes quantidades de insulina bastante pura. Depois disso, a insulina logo foi lançada no mercado.
Por esta descoberta marcante, Macleod e Banting foram agraciados com o Prêmio Nobel em Fisiologia em 1923. Banting, aparentemente insultado porque Best não fora mencionado, dividiu seu prêmio com ele, e Macleod imediatamente dividiu o seu com Collip. A patente da insulina foi vendida à Universidade de Toronto por um dólar.
A seqüência exata de aminoácidos contida na molécula de insulina, a chamada estrutura primária, foi determinada pelo biólogo britânico Frederick Sanger. Foi a primeira vez que a estrutura de uma proteína fora completamente determinada. Por isso, ele recebeu o Prêmio Nobel de Química em 1958. Em 1967, após décadas de trabalho, Dorothy Crowfoot Hodgkin determinou a conformação espacial da molécula mediante estudos de difração de raios X. Ela também recebeu um Prêmio Nobel.
12 de dezembro de 2011
9 de dezembro de 2011
O que é período de remissão, ou “LUA DE MEL”
O DM, diabetes mellitus da criança e do adolescente, é
uma doença crônica com insulino dependência. Ela decorre da destruição das
células beta do pâncreas por um processo auto imune. Antes da manifestação
clínica do DM, há um período sem sintomatologia que pode durar meses, ou mesmo
anos. Nesta fase é possível encontrar marcadores imunológicos. Quando as
alterações glicêmicas são observadas, já ocorreu a destruição de cerca de 80%
das células. É quando se inicia a terapia com insulina sub cutânea com objetivo
de estabilizar a doença. Em algum momento do surgimento da doença, geralmente
entre o segundo e sexto mês, já controlada com a insulinoterapia, cerca de 80%
das crianças entram em um período em que as necessidades de insulina diminuem,
muitas vezes chegando a zero. É o que se denomina período de remissão, ou fase
de "lua de mel".
Este período costuma durar algumas semanas,
meses e, às vezes, até um ano. A literatura especializada registra raras
situações nas quais a tolerância à glicose retorna ao normal, com peptídio-C
dosado no sangue demonstrando produção de pró insulina pelo pâncreas. Essa
ocorrência pode ser explicada pela cura de um processo inflamatório, acompanhado
de edema das ilhotas do pâncreas, com um número reduzido de células lesadas que
retomam sua função normal. Essa expectativa não deve ser alimentada em nossos
pacientes, pois são absolutamente excepcionais os casos de ocorrência dessa
"cura". Durante a fase de remissão há uma grande sensibilidade a pequenas doses
de insulina. Nessa fase praticamente não existem problemas e daí, ser chamada de
"lua de mel".
Tentativas foram feitas para prolongar essa
fase através do uso de medicação anti inflamatória sem lograr resultados
satisfatórios. Até hoje, a recomendação de tratamento mais adequada durante esse
período, é a da continuidade da insulinoterapia mesmo que aplicada em doses
mínimas. A suspensão poderia levar a uma falsa ilusão de uma cura que não vai
chegar. Além do mais, a criança e seus familiares podem abandonar práticas
saudáveis de alimentação, exercícios físicos e terem dificuldades posterior de
retorno. A dosagem de insulina aplicada durante esse período de remissão, ou
"lua de mel", precisa ser bem controlada para que sejam evitadas crises de
hipoglicemia.
Dra. Nuvarte Setian
Professora Associada de Pediatria FMUSP Chefe
da Unidade de Endocrinologia Pediátrica do Instituto da Criança do Hospital das
Clínicas da FMUSP
Fonte: www.portaldiabetes.com.br
8 de dezembro de 2011
INAUGURADO CENTRO DE HEMODIÁLISE NA APDP
No passado dia 14/11/2011, dia Mundial da Diabetes, foi inaugurado o Centro de Hemodiálise da Associação Protectora dos Diabéticos de Portugal (APDP). Este centro é exclusivamente dedicado a pessoas com Diabetes mellitus, tipo 1 ou tipo 2.
A hemodiálise neste novo centro foi concebida dentro da terapêutica integrada da Diabetes da APDP. Esta estratégia envolve a integração, na mesma estrutura, de diversas valências adequadas às complicações da Diabetes, nomeadamente cardiologia, endocrinologia, oftalmologia, podologia, urologia, psiquiatria, psicologia e nutrição.
O Centro localiza-se nas instalações da APDP, em Lisboa, estando equipado com a mais recente tecnologia.
Os programas de hemodiálise serão ajustados às complicações cardiovasculares de cada doente. Será incentivada a continuação da autonomia na terapêutica da doença renal crónica, com envolvimento no auto cuidado conforme a estratégia desenvolvida na APDP.
Com este novo projecto pretendemos contribuir para o melhor conhecimento do comportamento da Diabetes em diálise, e assim permitir individualizar a prestação de cuidados e melhorar a qualidade e a esperança de vida destes doentes.
Ver artigo original em: APDP
7 de dezembro de 2011
Medidor contínuo de glicose
Medidor contínuo de glicose SEM QUALQUER TIPO DE PERFURAÇÃO
Fundamentos da Espectroscopia Raman
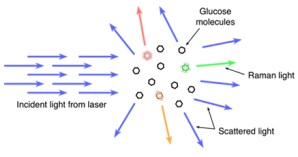
Se a luz de um único comprimento de onda (cor única) ilumina uma amostra, as moléculas desta amostra podem refletir, absorver ou espalhar a luz de alguma forma. Um número muito pequeno dos fótons incidente fará com que as moléculas vibrem ao espalhamento fora deles. A luz vai perder alguma energia durante essa interação, o que faz com que seja dispersa, com um comprimento de onda diferentes, ou cor. Isto é conhecido como o efeito Raman.Espalhamento Raman é um efeito muito fraco, não pode ser visto com os olhos ou detectado com uma câmera digital comum. Apenas cerca de um em 100 milhões de fótons de luz incidente irá produzir um único fóton-Raman espalhado. Os outros 99.999.999 fótons interagem com a amostra de outras formas, gerando uma grande quantidade de luz que deve ser eliminada a partir da medição, a fim de medir com precisão o sinal Raman.As cores gerados pelo espalhamento Raman são muito específicos para a estrutura química exata das moléculas da amostra. Formas das moléculas ”vários tamanhos, os átomos, e os tipos de ligações químicas vão gerar espectros Raman único que pode ser usado para identificar as moléculas específicas presentes.
A glicose é uma molécula relativamente grande que pode vibrar em muitos padrões diferentes, cada um dos quais pode causar luz Raman a ser gerada em diferentes cores. Esta exclusiva “impressão digital” espectral pode ser usado para medir sem ser invasiva o quanto de glicose está presente sob a pele.” Tradução do google!
A glicose é uma molécula relativamente grande que pode vibrar em muitos padrões diferentes, cada um dos quais pode causar luz Raman a ser gerada em diferentes cores. Esta exclusiva “impressão digital” espectral pode ser usado para medir sem ser invasiva o quanto de glicose está presente sob a pele.” Tradução do google!
“Figura 1: espalhamento Raman. Uma pequena parte da luz incidente fará com que as moléculas de glicose vibrem. A luz que espalha para fora destas moléculas que vibram terão cores diferentes do que a luz incidente devido ao efeito de Raman.”
Ver mais em: Minha Filha Diabética
Nova forma de medir os níveis de glicose
Os pesquisadores desenvolveram uma nova maneira de medir os níveis de glicose no sangue apenas iluminando uma região da pele com luz infravermelha. Crédito: cortesia de Patrick Gillooly.
Pesquisadores do Instituto Tecnológico de Massachusetts (MIT) estão desenvolvendo um dispositivo não invasivo, que utiliza luz para medir o nível de glicose no sangue. O aparelho poderá beneficiar milhões de pessoas com diabetes tipo 1, as quais são obrigadas a se picarem várias vezes ao dia para coletar sangue para o teste.
Idealizado pela primeira vez por Michael Feld, professor de física e ex-diretor do laboratório de espectroscopia do MIT, a técnica usa espectroscopia Raman, um método que identifica compostos químicos com base na frequência de vibrações das ligações que mantêm as moléculas unidas. A técnica pode revelar os níveis de glicose pela simples aproximação de luz infravermelha no braço ou no dedo, eliminando a necessidade das torturantes agulhas para coletar o sangue do paciente.
O aparelho de espectroscopia Raman, que está sendo desenvolvido pelos estudantes Ishan Barman e Chae-Ryon Kong, tem o tamanho de um laptop e poderá ser utilizado em um consultório ou na casa do paciente.
Os pesquisadores do laboratório de espectroscopia estão tentando desenvolver esta tecnologia faz 15 anos. Um dos principais obstáculos que eles têm enfrentado é o de que a luz infravermelha penetra apenas metade de um milímetro abaixo da pele. Assim, somente é possível fazer o registro do nível de glicose do fluido que banha as células da pele (conhecido como fluido intersticial), e não a quantidade no sangue. Para resolver este problema, a equipe utilizou um algoritmo que relaciona as duas concentrações, permitindo prever níveis de glicose no sangue pela concentração de glicose no fluido intersticial.
No entanto, esta calibração torna-se mais difícil imediatamente após o paciente comer ou beber algo doce, porque a glicose no sangue sobe rapidamente, enquanto no fluido intersticial leva de cinco a 10 minutos. Consequentemente, as medições de fluido intersticiais não dão uma imagem fiel do que está acontecendo na corrente sanguínea.
Para resolver esse tempo de latência, Barman e Kong desenvolveram um novo método de calibração, denominado Correção de Concentração Dinâmica (DCC, sigla em inglês), que incorpora a taxa na qual a glicose se difunde do sangue para o fluido intersticial.
Os pesquisadores descrevem o novo método de calibração e seu resultado na revista Analytical Chemistry.
6 de dezembro de 2011
Pâncreas Artificial

A diabetes mellitus do tipo 1 é considerada, por muitos médicos, como sendo a mais “ingrata”, porque é adquirida naturalmente e o paciente pode fazer muito pouco para tentar evitá-la. A vida do portador vira um eterno sobressalto, em que o nível de açúcar no sangue está sempre no topo da lista de preocupações. Mas as novas tecnologias parecem oferecer um alento: um pâncreas artificial.
O pâncreas de diabéticos do tipo 1 produz pouca ou nenhuma insulina. Sem ela, os níveis de açúcar ficam totalmente desregulados, e os problemas de saúde são graves e variados: tanto na falta quanto no excesso de glicose. Por isso, o paciente nunca tem sossego quando vai comer alguma coisa e precisa checar constantemente seus níveis de glicose.
O dispositivo artificial imita a função do pâncreas. Através de um sensor que se coloca embaixo da pele e mede o nível de glicose a todo o momento, um injetor de insulina dosa automaticamente a medida certa no corpo. Isso evita que o paciente precise manter suas taxas de açúcar sob controle permanente.
A novidade já vem sendo testada em vários lugares dos Estados Unidos, com sucesso. As autoridades americanas, no entanto, ainda não liberaram o dispositivo para produção de mercado por cautela. A saúde e a vida dos diabéticos dependem do nível de insulina, e uma falha técnica no aparelho, mesmo que breve, poderia causar danos irreversíveis.
Por essa razão, uma série de testes é necessária para que o pâncreas artificial possa ser usado com segurança. A expectativa é que a libertação por parte da Administração de Medicamentos e Alimentos (FDA, na sigla em inglês) já saia no começo de Dezembro. Mas os médicos afirmam que os pacientes, segundo as projeções, só poderão ter acesso a um pâncreas artificial daqui a um ano ou mais.
Artigo em: Portal Diabetes
Modelo para produzir célula-tronco abre caminho para regenerar fígado e pâncreas
Cientistas no Canadá superaram um obstáculo essencial na busca de tratamentos regenerativos para o diabetes e para a doença hepática com uma técnica capaz de produzir quantidades clinicamente úteis de células da endoderme a partir de células-tronco humanas pluripotentes.
"Um milhão de pessoas sofrem de diabetes tipo 1 nos Estados Unidos, enquanto a doença hepática soma 45 mil mortes por ano. Isso torna as células-tronco e o potencial para tratamentos regenerativos extremamente interessantes para os cientistas.
As técnicas de laboratório podem produzir milhares ou mesmo milhões destas células, mas gerá-las no número e na qualidade necessários para a medicina tem sido um desafio", explica o pesquisador Mark Ungrin, da University of Toronto.
A pesquisa enfocou o processo de usar células-tronco pluripotentes (PSC) para gerar as células da endoderme, uma das três camadas germinativas primárias que formam os órgãos internos, incluindo os pulmões, o pâncreas e o fígado.
A capacidade de transformar as PSCs em células da endoderme é um passo vital para o desenvolvimento de tratamentos regenerativos para estes órgãos.
"Para produzir a quantidade de células da endoderme necessária é importante compreender como as células se comportam em números maiores, por exemplo, quantas se perdem durante o processo de diferenciação e se todas as células vão se diferenciar nos tipos desejados", detalha Ungrin.
A equipe marcou as células com corante fluorescente e, enquanto elas se dividiam, o corante se segmentou igualmente entre as células.
Ao medir a fluorescência das populações de células em um estágio posterior, a equipe conseguiu descobrir a frequência da divisão celular, o que lhes permitiu prever quantas células estariam presentes em uma população em um dado momento.
Esta técnica permitiu que a equipe detectasse ineficiências celulares e desenvolvesse uma nova compreensão da biologia celular subjacente durante a diferenciação de PSCs. Isto permitiu que a equipe aumentasse a produção de células eficazes em 35 vezes.
"Nossos resultados mostraram um aumento significativo na quantidade de células da endoderme geradas. Este novo conceito nos permite ampliar a produção de células úteis, assegurando a sobrevivência das PSC e a diferenciação eficaz", disse Ungrin.
Superar esse gargalo na pesquisa também vai ajudar os futuros pesquisadores de células-tronco a navegar na rota muitas vezes longa e desafiadora entre os testes laboratoriais e o uso clínico, e acelerar o tempo entre o avanço biomédico e a terapia benéfica.
"A maioria das pesquisas nesta área se concentra na pureza das populações de células geradas. A eficiência de diferenciação continua não declarada.
No entanto, nossa pesquisa fornece um modelo importante para futuros estudos de células-tronco pluripotentes, particularmente onde as células terão de ser produzidas em quantidade para uso médico ou industrial", concluiu Ungrin.
Artigo em: FatimaNews
Subscrever:
Mensagens (Atom)